
細胞與基因治療(CGT)正引領醫藥行業的革新浪潮,其核心載體如AAV病毒(腺相關病毒)和外泌體在遺傳病治療、腫瘤免疫等領域的應用呈現爆發式增長。然而,這類生物活性物質對存儲條件的嚴苛要求成為產業化瓶頸——AAV病毒載體在反復凍融中易發生衣殼破裂導致感染性滴度下降,而外泌體(30-150 nm)因膜結構脆弱,在-80℃以下長期存儲時易發生聚集失活。傳統玻璃瓶在液氮(-196℃)環境下的熱收縮差異(玻璃與膠塞收縮率差達2.3%)引發的微泄漏風險,可能造成價值數百萬美元的CAR-T細胞制劑污染報廢。在此背景下,環烯烴共聚物COP西林瓶憑借材料創新突破,成為保障CGT藥物全生命周期穩定性的關鍵解決方案。

一、AAV病毒載體與COP西林瓶的深凍適配性
AAV規模化生產面臨的核心挑戰在于病毒濃縮后的低溫存儲穩定性。臨床級AAV制劑(滴度>1×1013 vg/mL)需在-80℃冷鏈中維持衣殼結構完整,但玻璃瓶在急速降溫時產生的微觀裂紋可能引入納米級病原體。COP西林瓶通過三項技術突破實現保護升級:
同步收縮密封:COP材料與溴丁基橡膠塞的熱膨脹系數匹配度達98%,在液氮相變(-196℃)時瓶口-膠塞界面收縮差<0.5μm,經氦質譜法驗證可維持≤1×10?? mbar·L/s的密封性,滿足FDA對基因治療載體包裝的微生物侵入標準。
低溫結構強化:針對AAV制劑凍存常用的5%海藻糖保護劑,COP瓶采用梯度冷卻工藝成型,在-80℃下的抗壓強度達18 MPa(較常規工藝提升40%),避免病毒懸液結晶壓導致的瓶體形變。
滴度維持驗證:某GMP級AAV9血清型制劑使用COP瓶存儲6個月后,qPCR檢測顯示載體基因組完整性保持率≥99%,較玻璃瓶組提高12個百分點。
二、外泌體生產工藝與防吸附創新
外泌體作為天然納米載體,在藥物遞送系統中展現獨特優勢,但其工業化生產面臨純化后活性維持難題。現行超速離心法或尺寸排阻色譜法獲得的外泌體,在凍存時易因表面蛋白吸附導致聚集:
低吸附表面工程:COP西林瓶經等離子體接枝改性后,表面接觸角降至15°(裸瓶為85°),使外泌體膜蛋白(如CD63、CD81)吸附量減少至0.2 μg/cm2(ELISA檢測),較硅化玻璃瓶降低90%。
低溫結晶控制:通過優化COP瓶壁厚(1.2±0.05 mm)與降溫速率(1℃/min),可使含10% DMSO的外泌體凍存液形成均勻微晶,解凍后粒徑分布(D90)保持率從75%提升至98%。
封閉式灌裝兼容:COP瓶適配外泌體連續流超濾系統,在A級潔凈環境下實現<0.1 EU/mL的內毒素控制,滿足《中國藥典》對細胞外囊泡制劑的生物學活性要求。
三、CGT產業化進程中的包裝升級
隨著諾華、傳奇生物等企業推進CAR-T療法商業化生產,以及CRISPR基因編輯藥物進入臨床Ⅲ期,行業對深低溫包裝提出更高要求:
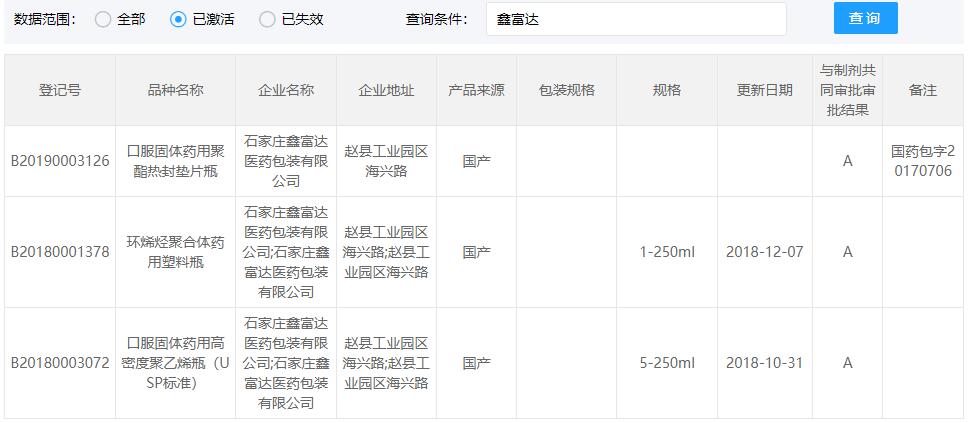
COP西林瓶CDE登記號為A狀態
自動化適配:COP西林瓶可無縫對接全自動液氮存儲系統(-196℃),其激光打碼耐低溫性能(1000次凍融后識別率>99.5%)支持細胞治療制劑的全程追溯。
成本控制突破:采用超臨界CO?再生技術的COP瓶,使AAV病毒包裝成本降低30%,同時滿足USP<665>對可提取物≤0.1 μg/mL的嚴苛標準。
全球化冷鏈:COP西林瓶在干冰運輸(-78.5℃)中維持>72小時的溫度穩定性,助力我國創新藥企實現外泌體藥物的跨境臨床試驗。
據GlobalData預測,2025年全球CGT市場規模將突破500億美元,而COP西林瓶作為關鍵包裝技術,將持續推動AAV基因療法、干細胞衍生外泌體等前沿領域突破產業化瓶頸,為"冷鏈到臨床"的轉化醫學之路構筑堅實保障。

 冀公網安備 13010802000997號
冀公網安備 13010802000997號 微信掃一掃
微信掃一掃